루게릭병에 대한 이해
루게릭병 유전자, 어느 정도 유전될까?
로뎀요양병원
유재국 병원장
산발형 루게릭병(Sporadic ALS, SALS)과 가족형 루게릭병(Familal ALS, FALS).
루게릭병에 걸린 환우들이나 환우 가족들의 고민은 항상 한가지가 더 있다. “형제, 자식들도 이 병에 걸릴 가능성은 어떤가요? 유전되는 병인가요?” 필자도 이때 참 대답하기가 어렵다. 모든 병이 이제는 유전자의 연계관계가 아예 없는 질환은 없다고 볼 수 있는 시대이다보니 가족성루게릭병과 산발형 루게릭병의 경계를 나눈다는 것이 조심스러운 면이 있다. 가족성 루게릭병의 진단에 있어 참고가 되는 유전자가 산발형 루게릭병에서도 관찰될 수 있기 때문에 무조건 맞다고, 무조건 아니라고 말하기도 어렵기 때문이다. 다만 확률적으로 혈액형처럼 결정적인 형태의 유전은 아니라고 설명드리고, 확률상 가족성 루게릭병의 경우는 5% 안쪽으로 낮은 편이라고 일단 안심시킨다.
여기서 우리가 늘 접하면서도 막상 정확히 구분해 쓰기는 어려운 유전병(Hereditary)과 유전성질환(gentic), 뭐가 다른지부터 정리해둘 필요가 있다. 유전병은 ‘선천적 장애’로 분류된다. 유전으로 인한 선천적 장애는 부모로부터 대물림되지만, 출생 시부터 장애를 동반하는 것은 아니다. 선천적 장애는 신생아의 2~4%에서 발생하며 대부분 염색체이상질환이고 단일유전자에 의한 유전병은 약 60000여종이 알려져 있다. 예를 들어 21번 염색체가 세개로 체세포에 47개의 염색체가 관찰되는 다운증후군과 같은 경우가 이에 해당된다. 이에 반해 유전성질환은 유전자결합, 유전자돌연변이, 음주, 흡연 등 여러 가지 요인이 복합적으로 작용해 발생하기 때문에 ‘다인자성유전질환’이라고 불린다. 다인자성 유전질환은 기형, 정신질환, 고혈압, 당뇨병, 암 등 헤아릴 수 없이 많다.
루게릭병도 이렇게 보면 다양한 유전자가 상호작용을 통해 혹은 여러 가지 환경요소가 복합적으로 작용할 수 있으므로 다인자성 유전질환으로 볼수 있다. 그리고 유전자에 대한 검사는 향후의 맞춤형 유전자 치료법이 개발된다는 것을 가정할 때 이에 대한 검사는 필요하다고 생각된다. 또한 유전자적인 차이가 치료제에 대한 반응이나 인지기능의 차이와도 연관이 있다고 알려져 있어 이에 대한 평가는 필요하며 대다수 대학병원에서 유전자검사를 병행하곤 한다.
루게릭병의 발병원인은 환경적 요인과 유전적인 원인 등이 제시되고 있는데, ALS 환자의 약 3~10%에서 가족력이 보고되는 가족성 ALS (Familial ALS)이라는 점과 1993년 Cu/Zn-binding superoxide dismutase (SOD1) 유전자 돌연변이가 일부 가족성 루게릭병 환자에서 밝혀짐에 따라 유전적인 원인에 대한 많은 연구가 진행되었다. 그 결과 50개 이상의 ALS 유전자좌(locus)가 밝혀졌고, 하단의 표1에서 나열된 다양한 유전자들이 지속적으로 밝혀지고 있다.
표1. 루게릭병 유전자명과 해당 단백질명, 그리고 기능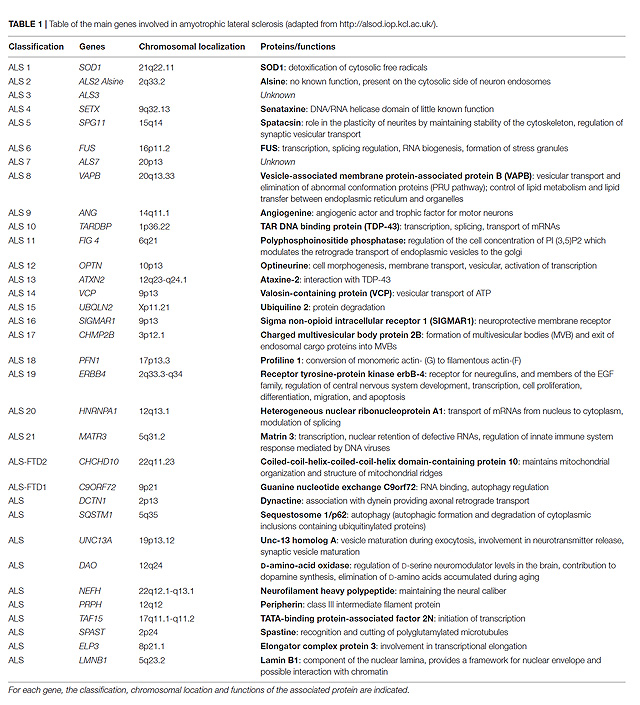
외국에서는 ALS 환자 중 5~10%에서 가족력이 있는 FALS 환자라고 알려졌고, FALS 환자 중 약 20%에서 SOD1 유전자 돌연변이가 발견되고 있다. 주로 한국에서 일단 진행해보게 되는 유전자검사는 SOD1 유전자이긴 하며 약 4%와 1-4%의 환자들에서는 FUS 유전자와 TARDBP 유전자 돌연변이가 각각 보고되고 있다. 또한, 가족력이 없는 산발성 ALS (sporadic ALS; SALS)의 약 2-4%에서도 SOD1 유전자 돌연변이가 발견된다고 한다. 우리나라의 경우 SOD1 돌연변이가 발견된 가계는 다수 보고되고 있으나, FALS 및 SALS에서 돌연변이 빈도에 대한 보고는 없는데, 2011년 한양대학교병원 루게릭병클리닉 의료진과 공동연구로 250명 이상의 ALS 환자에 대한 유전자 분석 결과 우리나라에는 FALS 환자의 비율은 5% 미만으로 낮은 반면 FALS 환자들에서의 SOD1 및 FUS 유전자 돌연변이가 각각 78%와 11%로 발견되어 매우 높은 양성률을 보였다. 또한, SALS에서도 약 5% 정도에서 SOD1, FUS를 비롯하여 PON1, PON2, PON3 등의 유전자 이상이 발견되었다. 이후에도 하단의 그래프와 같이 계속, 보고가 이어지고 있다.
그래프 > 시계열로 보고된 루게릭병 유전자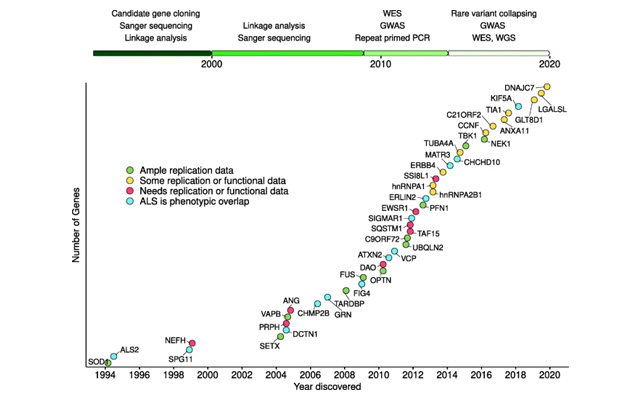
그래서 많은 사람이 유전자 관련 발견 뉴스를 접하면 신약발표에 버금가는 정도로 관심이 많았다. 왠지 이 병을 이제는 훨씬 더 이해할 수 있는 단계로 가고 있다고 생각했다. 그러나 루게릭병 유전자는 계속 숫자가 늘어갈수록 미궁에 빠지는 면도 있는, 참 복잡한 질환 같다. 유전자에 대한 연구가 꽤나 많이 진행되어 발표되는 유전자들은 늘어가고 있으나 진료하는 입장에서는 갈수록 복합질환의 성격을 시사하는 면이 크다 보니 완벽한 치료제 개발이 더 어려운 것은 아닌지 고민되기도 한다.
그동안 루게릭병 하면 대체로는 유전이 안 되는 루게릭병이 대부분이고 드물게 가족형 루게릭병이 보고되고는 했다. 루게릭병 유전자가 직계 가족에서 동시에 관찰되면 가족형으로 보고하곤 했다. 예를 들면 SOD1 유전자가 어머니와 아들에서 동시에 검출된다면 가족형 루게릭병이라는 식으로 말이다. 그러나 다시 언급하지만, 예를 들어 ANXA11 유전자 돌연변이가 관찰되었다고 해당환자를 가족형 루게릭병(FALS)으로 단정 지을 수는 없다. 해당질환의 발병에 관여한 유전자를 확인했을 뿐 이 유전자가 우성유전이 될지, 열성유전이 될지, 기타유전이 될지는 각각 다르고 복잡하다.
기존 논문들에 따르면 루게릭병 환자 중 5~10%는 특정 유전자에 변이가 일어난 것이 원인인 가족성 루게릭병(Familial ALS)을 앓고 있다. 한국 논문에 따르면 3~4% 선으로 더 적게 보고한 바도 있다. 실제로 부모로부터 자녀에게 변이된 유전자가 전달되면서 질환이 유발될 수 있지만 모든 루게릭병 환자의 자녀가 같은 질환을 겪지는 않으며, 어떤 유전자 변이를 전달받았는지에 따라 자녀가 질환을 겪을 수도 있는 확률이 달라진다.
유전형과 산발형 루게릭병 모두 변이된 유전자에 따라 증상의 시작부위, 발병 시점, 진행 정도 등이 다를 수 있다. 이렇게 되면 모두 유전자와의 상관성이 있는 유전성 질환이라고 해야 할 수도 있다. 혈액형과 같이 직접적인 유전성향이 확고하게 적용되는 상황인지 아니면 조금 더 걸릴 확률이 높은 상태이냐의 질문이 된다.
현재 세계적으로 보고된 가족성 루게릭병의 양상은 40%는 C9ORF72 유전자 결함에서, 10~20%는 SOD1 유전자의 돌연변이로 인해 발생한다. 다만, 이것도 인종에 따라서도 다른 결과가 나오고 있다. 쉽게 말해 우리나라 환자들과 미국이나 유럽의 서구사람들과 유전자양상이 다르다. 어떤 한 유전자를 고쳐내는 방식의 유전자 치료방식이 아닌, 다수의 유전자들이 각각의 발현 비율이 다르고 표출방식이 다르게 나타나고 있다는 사실이 수차례 논문으로 발표된 바 있다. 즉 서구에서는 전두엽성 치매를 동반하는 것으로 알려진 C9Orf72라는 유전자가 가장 많은 빈도를 갖고 있으나 우리나라는 이런 환자들은 약 260명의 환자를 통해 분석했을 때 전혀 발견되지 않았다고 한다.
반면, SOD1, FUS 유전자는 서구보다 많은 비율로 발견되었다. 그 빈도는 모든 환자 중 3~5% 미만에서 발견되었으므로 대부분의 루게릭병은 가족에게 나타나는 유전형이라기보다는 가족에서 같은 질환이 확인되지 않는 산발형으로 생각하게 되었다. SOD1 유전자에 기인한 가족형 루게릭병은 결국 직계 가족의 검사를 통한 유전자의 동반검출 및 동반 증상, 신경생리검사 결과 확인 외에는 현재로서는 진단이 어려운 것도 사실이다. 그러나 다양한 유전자가 상호작용을 통해 혹은 여러 가지 환경요소가 복합적으로 작용할 수 있으므로 유전자에 대한 검사는 향후의 맞춤형 유전자 치료법이 개발된다는 점을 가정할 때 이에 대한 검사는 필요하다고 생각된다. 적어도 SOD1유전자(SOD1 유전자는 체내 구리와 아연 분자에 결합하는 효소를 만드는 기능이 있는데, 인체에 독성 분자로 작용하는 초과산화물 라디칼(superoxide radical)을 분해하는 역할을 한다)만큼은 유전자 치료제(큐알소디, QALSODY, 토퍼센 등) 의 개발도 이루어져 FDA 판매승인을 받았던 만큼 확인해보는 것도 나쁘지 않다. 또한 유전자적인 차이가 치료제에 대한 반응이나 인지기능의 차이와도 연관이 있다고 알려졌으므로 이에 대한 평가는 나름 필요하다.
전방위 유전자 검사를 시행할 경우 환자와 가족들에게 정확한 정보를 전달하는 것은 매우 중요하다. 루게릭병의 경우 상염색체 우성(autosomal dominant), 상염색체 열성(autosomal recessive), X-염색체 유전(X-linked) 등 다양한 양상으로 유전될 수 있으며, 가족성 루게릭병(FALS) 의 경우 특정 유전자 돌연변이가 발견되면 동일 가계에서 발생한 환자들은 동일한 유전자 돌연변이를 가지고 있다. 산발형루게릭병(SALS)의 경우 유전자 돌연변이가 발견되었다면 가능한 부모에 대한 검사를 시행하여 새로 발생한(de novo) 돌연변이인지, 낮은 투과도(penetrance)에 의해 환자에게서만 발병한 경우인지 확인하여야 한다. 만약 새로 발생한 돌연변이라면 환자의 부모나 형제에서 ALS가 발생할 가능성은 매우 낮지만, 환자의 자녀는 50%의 확률로 유전자 돌연변이를 물려받게 되고 질환 발생의 가능성도 높아진다. 그렇지만, 아직 완치약이 준비되지 않은 질환에서 증상이 없는 환자의 가족들에서 전방위적 다수 유전자 검사를 시행하는 것이 바람직한가에 대해서는 아직 논란이 많다. 유전자 검사의 장점과 단점, 이익과 불이익에 대한 정보를 충분히 제공한 후 검사 여부를 결정하도록 하여야 한다.
한번은 정리해 드리고 싶은 내용이어서 오랜만에 타이프를 치게 되었다. 해당 질환의 유전양상을 고려할 때 줄기세포치료를 통한 접근이 타당하다는 사실에 공감한다. 다만 비용이 너무 고가인지라 늘 고민이 함께 가는 어느 날 밤이다. 오늘도 루게릭 환우와 환우 가족들에게 평안한 밤이 찾아오길 바라며.
참고> 그래도 한국에서 가장 많이 조사하는 루게릭 유전자 SOD1 유전자
가장 먼저 발견된 유전자로 알려진SOD1은 1993년에 이미 루게릭병(amyotrophic lateral sclerosis, ALS) 발병과 밀접한 연관이 있고 이 질환의 중요한 병원성 유전자라는 사실을 발견했다. 또한 가족성 ALS에도 해당 유전자의 돌연변이가 존재하며 이러한 돌연변이가 엑손(Exon)에서 많이 발생하여 SOD1이 단백질을 암호화하는 기능을 상실하게 된다. 이밖에 SOD1의 일부 돌연변이는 그 자체에 Aβ와 같은 응집을 더 쉽게 생성되게 하며 소수의 돌연변이 단백질은 프리온과 같이 동일한 세포 내의 정상 단백질도 더 쉽게 집결되게 할 수 있다. 이러한 비정상적인 SOD1 응집을 가진 세포들은 다른 기존의 정상적인 세포를 변형시켜 그 세포 내 SOD1도 응집이 발생하게 한다.
참고문헌 :
1> Genetics of Amyotrophic lateral sclerosis, Neurogenetics and Psychiatric Genetics (C Cruchaga and C Karch, Section Editors) Published: 07 November 2020 volume
2> Identification of mutations in Korean patients with amyotrophic lateral sclerosis using multigene panel testing Neurobiol Aging. 2016 Jan;37:209.e9-209.e16. doi: 10.1016/j.neurobiolaging.2015.09.012. Epub 2015 Sep 30.
3> Clinical testing panels for ALS: global distribution, consistency, and challenges, Amyotroph Lateral Scler Frontotemporal Degener. 2023 Aug;24(5-6):420-435. doi: 10.1080/21678421.2023.2173015. Epub 2023 Mar 10.
본원에서 치료받고 계신 300명이 넘는 루게릭병(근위축측삭경화증)환자들과 다수의 신경계희귀난치성 질환 환자들, 그리고 기타 희귀 내과계 질환, 독성질환을 가지고 계신 난치성 환자들의 진료과정을 통하여 루게릭병과 각종 희귀질환 치료 방향에 대한 의견을 전합니다.
