미국 식품의약국(FDA)이 인튜이티브 서지컬 로봇 수술 시스템 '다빈치(da Vinci)'에 쓰이는 특정 스테이플러 리로드 제품에 대해 사용 중단을 권고하는 조기 경보를 발령했다. 해당 기기 결함으로 최근 환자 1명이 사망하고 4명이 중상을 입은 데 따른 조치다.
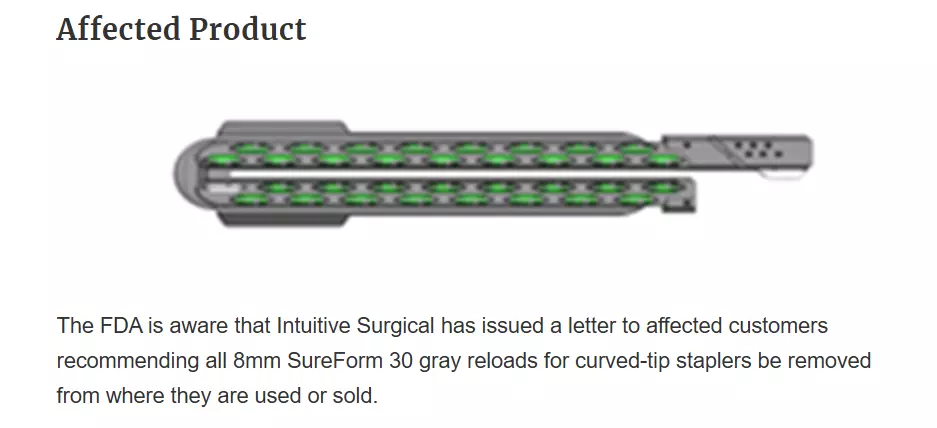
23일 관련 업계에 따르면 FDA는 인튜이티브 서지컬 다빈치용 '8mm 슈어폼 30 회색 리로드(8mm SureForm 30 Gray Reload)'를 사용하는 고객들에게 해당 제품을 즉시 폐기하거나 수거할 것을 권고했다.
이번 경보는 혈관 등에 스테이플 라인이 불완전하게 형성되는 결함이 보고되면서 내려졌다. FDA에 따르면 스테이플이 제대로 박히지 않을 경우 조직이 절단된 상태에서 혈관 내부가 그대로 노출돼 심각한 출혈을 유발할 수 있다. 이 경우 로봇 수술을 즉시 중단하고 긴급히 개복 수술로 전환해야 하는 위험이 뒤따른다.
회수 대상 제품은 일반 외과를 비롯해 흉부외과, 산부인과, 비뇨기과, 소아외과 등에서 혈관 및 조직 절제와 문합(장기나 혈관의 연결)을 위해 쓰여 왔다. 지난 2월 23일 기준 해당 결함과 관련해 1건의 사망 사례와 4건의 중상 사례가 확인됐으며 회사 측은 지난 3월 11일 고객 서한을 발송해 문제가 된 제품 사용을 즉시 중단할 것을 요청하고 대체 제품으로 전환할 것을 권고했다.
FDA는 현재 이번 사안을 고위험 기기 문제로 간주하고 관련 정보를 검토 중이며 조사 진행에 따라 추가 정보를 업데이트할 계획이다.
23일 관련 업계에 따르면 FDA는 인튜이티브 서지컬 다빈치용 '8mm 슈어폼 30 회색 리로드(8mm SureForm 30 Gray Reload)'를 사용하는 고객들에게 해당 제품을 즉시 폐기하거나 수거할 것을 권고했다.
이번 경보는 혈관 등에 스테이플 라인이 불완전하게 형성되는 결함이 보고되면서 내려졌다. FDA에 따르면 스테이플이 제대로 박히지 않을 경우 조직이 절단된 상태에서 혈관 내부가 그대로 노출돼 심각한 출혈을 유발할 수 있다. 이 경우 로봇 수술을 즉시 중단하고 긴급히 개복 수술로 전환해야 하는 위험이 뒤따른다.
회수 대상 제품은 일반 외과를 비롯해 흉부외과, 산부인과, 비뇨기과, 소아외과 등에서 혈관 및 조직 절제와 문합(장기나 혈관의 연결)을 위해 쓰여 왔다. 지난 2월 23일 기준 해당 결함과 관련해 1건의 사망 사례와 4건의 중상 사례가 확인됐으며 회사 측은 지난 3월 11일 고객 서한을 발송해 문제가 된 제품 사용을 즉시 중단할 것을 요청하고 대체 제품으로 전환할 것을 권고했다.
FDA는 현재 이번 사안을 고위험 기기 문제로 간주하고 관련 정보를 검토 중이며 조사 진행에 따라 추가 정보를 업데이트할 계획이다.