국내연구팀이 세계 최초로 레버씨 시신경 위축증 유전자 교정 치료에 성공했다.
레버씨 시신경 위축증(LHON)은 모계유전되는 미토콘드리아 질환으로, 시신경세포가 퇴행해 빠르게 중심시야를 잃고 실명으로 이어진다. 주로 10~30대 젊은 남성에게서 발병하고, 전 세계적으로 약 3만~5만 명 이상이 시력을 잃는 주요 유전성 시신경 질환이다. 아직 유전자를 교정하는 등 근본적인 치료제는 없는 실정이었다.
고려대 의대 융합의학교실 이현지 교수 연구팀이 서울대 수의과대학, 주식회사 엣진과 공동연구를 통해 유전변이를 교정했다.
LHON의 원인은 미토콘드리아 DNA(mtDNA) 내 MT-ND4, ND1, ND6 등 복합체 I 유전자의 점 돌연변이다. 그 중, MT-ND4의 m.G11778A 변이가 전체 환자의 약 70%를 차지한다. 그러나 미토콘드리아 내부에는 일반적인 CRISPR 유전자 가위의 가이드 RNA가 진입하지 못하기 때문에 유전자 치료가 불가능했다. 현재 승인된 유일한 치료제인 이데베논도 미토콘드리아 기능을 일시적으로 보조할 뿐 근본적인 치료 효과는 제한적이었다.
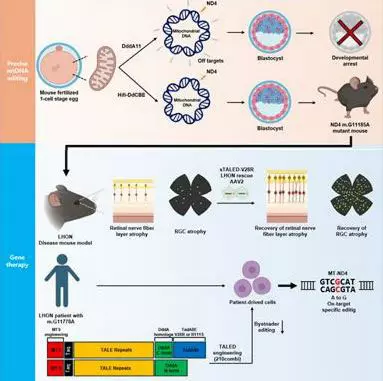
연구팀은 미토콘드리아 염기교정 기술인 'Hifi-DdCBE'를 이용해 사람 LHON 변이와 대응되는 MT-ND4 G11778A 변이(m.G11185A)를 생쥐에서 정밀하게 구현했다. 이 모델은 망막 시신경층 두께 감소, 시신경세포 수 감소, 시기능 저하 등 실제 LHON 환자와 동일한 병리적 특징을 보였다.
이후 연구팀은 지난 2024년 Cell 논문에 보고했던 변이 mtDNA를 정상 염기로 교정하는 치료법을 적용했다. 정밀도 향상형 'TALE-linked deaminase(TALED-V28R)'를 이용해 AAV(아데노부속바이러스)로 전달했다. 유리체 내 주사로 주입된 AAV-TALED V28R은 시신경세포의 병인 유전변이를 교정했다. 망막 두께와 시신경세포 수가 정상 수준으로 회복됐고 시각 기능(OKN·ERG 검사) 또한 유의미하게 개선됐다.
연구팀은 TALED V28R을 LHON 환자 유래 세포에도 적용했다. 그 결과, ATP 생성과 미토콘드리아 복합체 I 활성이 회복됐다.
공동 제1저자인 고려대 의대 김상훈 박사과정생은 “치료제의 부재로 고통받고 있는 환자들에게 새로운 가능성과 희망이 생길 것”이라며 “앞으로 미토콘드리아 유전자 교정 기술을 더욱 발전시켜, 실제 임상 현장에서 활용될 수 있도록 연구에 매진하겠다”고 말했다.
공동 연구책임자인 고려대 의대 융합의학교실 이현지 교수는 “이번 연구는 세계 최초로 미토콘드리아 질환 생체 모델에서 유전자 교정 치료 효과를 실증한 연구”라며 “앞으로 레버씨 시신경 위축증을 비롯해 다양한 미토콘드리아 유전질환의 유전자 교정 치료제가 임상적 적용 단계로 도약해 실제 치료제로 상용화되기를 기대한다”고 말했다.
한편, 이번 연구는 세계적 국제학술지인 'Nature Communications'(IF=15.7)에 최근 게재됐다.
레버씨 시신경 위축증(LHON)은 모계유전되는 미토콘드리아 질환으로, 시신경세포가 퇴행해 빠르게 중심시야를 잃고 실명으로 이어진다. 주로 10~30대 젊은 남성에게서 발병하고, 전 세계적으로 약 3만~5만 명 이상이 시력을 잃는 주요 유전성 시신경 질환이다. 아직 유전자를 교정하는 등 근본적인 치료제는 없는 실정이었다.
고려대 의대 융합의학교실 이현지 교수 연구팀이 서울대 수의과대학, 주식회사 엣진과 공동연구를 통해 유전변이를 교정했다.
LHON의 원인은 미토콘드리아 DNA(mtDNA) 내 MT-ND4, ND1, ND6 등 복합체 I 유전자의 점 돌연변이다. 그 중, MT-ND4의 m.G11778A 변이가 전체 환자의 약 70%를 차지한다. 그러나 미토콘드리아 내부에는 일반적인 CRISPR 유전자 가위의 가이드 RNA가 진입하지 못하기 때문에 유전자 치료가 불가능했다. 현재 승인된 유일한 치료제인 이데베논도 미토콘드리아 기능을 일시적으로 보조할 뿐 근본적인 치료 효과는 제한적이었다.
연구팀은 미토콘드리아 염기교정 기술인 'Hifi-DdCBE'를 이용해 사람 LHON 변이와 대응되는 MT-ND4 G11778A 변이(m.G11185A)를 생쥐에서 정밀하게 구현했다. 이 모델은 망막 시신경층 두께 감소, 시신경세포 수 감소, 시기능 저하 등 실제 LHON 환자와 동일한 병리적 특징을 보였다.
이후 연구팀은 지난 2024년 Cell 논문에 보고했던 변이 mtDNA를 정상 염기로 교정하는 치료법을 적용했다. 정밀도 향상형 'TALE-linked deaminase(TALED-V28R)'를 이용해 AAV(아데노부속바이러스)로 전달했다. 유리체 내 주사로 주입된 AAV-TALED V28R은 시신경세포의 병인 유전변이를 교정했다. 망막 두께와 시신경세포 수가 정상 수준으로 회복됐고 시각 기능(OKN·ERG 검사) 또한 유의미하게 개선됐다.
연구팀은 TALED V28R을 LHON 환자 유래 세포에도 적용했다. 그 결과, ATP 생성과 미토콘드리아 복합체 I 활성이 회복됐다.
공동 제1저자인 고려대 의대 김상훈 박사과정생은 “치료제의 부재로 고통받고 있는 환자들에게 새로운 가능성과 희망이 생길 것”이라며 “앞으로 미토콘드리아 유전자 교정 기술을 더욱 발전시켜, 실제 임상 현장에서 활용될 수 있도록 연구에 매진하겠다”고 말했다.
공동 연구책임자인 고려대 의대 융합의학교실 이현지 교수는 “이번 연구는 세계 최초로 미토콘드리아 질환 생체 모델에서 유전자 교정 치료 효과를 실증한 연구”라며 “앞으로 레버씨 시신경 위축증을 비롯해 다양한 미토콘드리아 유전질환의 유전자 교정 치료제가 임상적 적용 단계로 도약해 실제 치료제로 상용화되기를 기대한다”고 말했다.
한편, 이번 연구는 세계적 국제학술지인 'Nature Communications'(IF=15.7)에 최근 게재됐다.