
식품의약품안전처는 국가 R&D로 개발하고 있는 세포기반 인공혈액을 첨단바이오의약품으로 분류했다고 8일 밝혔다. 이로써 임상시험 진입, 품목허가 신청 등 향후 개발과정의 본격적인 진행이 가능해졌다.
세포기반 인공혈액 기술개발사업은 저출생·고령화와 감염병 발생 등으로 인한 혈액 공급난 대비를 위해 줄기세포로부터 적혈구, 혈소판을 생산하고 상용화하는 기술 확보를 목표로 2023년도부터 추진하고 있는 사업이다. 총 사업규모 약 481억원으로, 복지부·과기부·산업부·식약처·질병청이 함께 참여하고 있다.
세포기반 인공혈액은 세계적으로 제품화 사례가 없는 신개념 제품으로 가이드라인 등 규제체계가 미비하고, 국내 '혈액관리법'은 인체에서 채혈한 혈구 및 혈장만을 ‘혈액’으로 규정하고 있어 안전성과 효과성 평가방법 등 제품화를 위한 규제요건이 불명확한 상황이었다.
식약처는 2024년부터 규제정합성 검토 제도를 통해 개발 초기단계부터 제품화에 필요한 규제 요건과 대응 전략 등 컨설팅을 제공해왔다. 제품의 사용 목적, 형태, 작용 기전 등을 종합적으로 검토해 세포기반 인공혈액(적혈구, 혈소판)을 '첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률'에 따른 ‘첨단바이오의약품’으로 분류를 결정했다.
세포기반 인공혈액 기술개발사업은 저출생·고령화와 감염병 발생 등으로 인한 혈액 공급난 대비를 위해 줄기세포로부터 적혈구, 혈소판을 생산하고 상용화하는 기술 확보를 목표로 2023년도부터 추진하고 있는 사업이다. 총 사업규모 약 481억원으로, 복지부·과기부·산업부·식약처·질병청이 함께 참여하고 있다.
세포기반 인공혈액은 세계적으로 제품화 사례가 없는 신개념 제품으로 가이드라인 등 규제체계가 미비하고, 국내 '혈액관리법'은 인체에서 채혈한 혈구 및 혈장만을 ‘혈액’으로 규정하고 있어 안전성과 효과성 평가방법 등 제품화를 위한 규제요건이 불명확한 상황이었다.
식약처는 2024년부터 규제정합성 검토 제도를 통해 개발 초기단계부터 제품화에 필요한 규제 요건과 대응 전략 등 컨설팅을 제공해왔다. 제품의 사용 목적, 형태, 작용 기전 등을 종합적으로 검토해 세포기반 인공혈액(적혈구, 혈소판)을 '첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률'에 따른 ‘첨단바이오의약품’으로 분류를 결정했다.
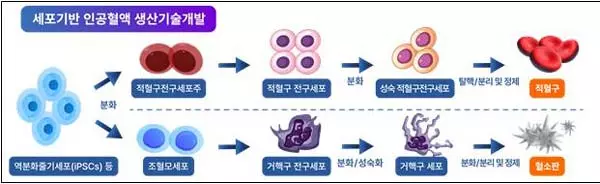
이번 품목분류로 평가기준 대비 및 임상시험 진입, 허가 신청 등이 가능해졌으며, 향후 개발과정이 정상적으로 완료되면 헌혈 혈액을 대체하는 것 외에도 희귀혈액형, 혈소판 감소증 환자 등 특수 수요에도 대응할 수 있을 것으로 기대된다.
식약처는 "이번 사례가 규제기관이 국가 혁신 R&D 초기단계부터 기술과 규제의 정합성을 검토하면서 기존 규제의 틀에 맞지 않는 신개념 제품에 규제의 길을 제시해 불확실성을 해소하고 개발을 이어갈 수 있도록 지원한 의미가 크다"고 했다.
식약처는 "이번 사례가 규제기관이 국가 혁신 R&D 초기단계부터 기술과 규제의 정합성을 검토하면서 기존 규제의 틀에 맞지 않는 신개념 제품에 규제의 길을 제시해 불확실성을 해소하고 개발을 이어갈 수 있도록 지원한 의미가 크다"고 했다.